I.Pendahuluan
Kebanyakan
orang memahami benar mengenai pentingya
pengukuran pencemaran udara. Kebanyakan orang awam tidak mengetahui tentang
pengukuran-pengukuran teliti yang harus terlebih dahulu dilakukan agar dapat
melaksanakan pengendalian secara efektif.
Pengukuran-pengukuran itu penting,pertama untuk menetapkan tingkat
pencemaran udara yang dapat diterima dengan memperhatikan data biologi yang
relevan pada manusia dan hewan. Kedua,pengukuran itu perlu dilakukan berbagai
tempat untuk menentukan sumber-sumber pencemaran dan derajat pengendalian yang
diperlukan. Pencemaran udara
adalah kehadiran satu atau lebih substansi fisik,
kimia, atau biologi di atmosfer dalam jumlah yang dapat
membahayakan kesehatan manusia, hewan, dan tumbuhan, mengganggu estetika dan
kenyamanan, atau merusak properti. Pencemaran
udara dapat ditimbulkan oleh sumber-sumber alami maupun kegiatan manusia.
Beberapa definisi gangguan fisik seperti polusi suara, panas,
radiasi atau polusi cahaya dianggap sebagai polusi
udara. Sifat alami udara mengakibatkan dampak pencemaran udara dapat bersifat
langsung dan lokal,
regional, maupun global. Kelembaban udara bergantung pada
konsentrasi uap air, dan H2O yang berbeda-beda konsentrasinya di setiap daerah.
Kondisi udara di dalam atmosfer tidak pernah ditemukan dalam keadaan
bersih, melainkan sudah tercampur dengan gas-gas lain dan partikulat-partikulat
yang tidak kita perlukan. Gas-gas dan partikulat-partikulat yang berasal dari
aktivitas alam dan juga yang dihasilkan dari aktivitas manusia ini
terus-menerus masuk ke dalam udara dan mengotori/mencemari udara di lapisan
atmosfer khususnya lapisan troposfer. Apabila bahan pencemar
tersebut dari hasil pengukuran dengan parameter yang telah ditentukan oleh WHO
konsentrasi bahan pencemarnya melewati ambang batas (konsentrasi yang masih
bisa diatasi), maka udara dinyatakan dalam keadaan tercemar. Pencemaran udara
terjadi apabila mengandung satu macam atau lebih bahan pencemar diperoleh dari
hasil proses kimiawi seperti gas-gas CO, CO2, SO2, SO3, gas dengan konsentrasi
tinggi atau kondisi fisik seperti suhu yang sangat tinggi bagi ukuran manusia,
hewan dan tumbuh-tumbuhan. Adanya gas-gas tersebut dan partikulat-partikulat
dengan konsentrasi melewati ambang batas, maka udara di daerah tersebut
dinyatakan sudah tercemar. Dengan menggunakan parameter konsentrasi zat
pencemar dan waktu lamanya kontak antara bahan pencemar atau polutan dengan
lingkungan (udara), WHO menetapkan empat tingkatan pencemaran sebagai berikut:
- Pencemaran tingkat pertama; yaitu pencemaran yang tidak menimbulkan kerugian bagi manusia.
- Pencemaran tingkat kedua; yaitu pencemaran yang mulai menimbulkan kerugian bagi manusia seperti terjadinya iritasi pada indra kita.
- Pencemaran tingkat ketiga; yaitu pencemaran yang sudah dapat bereaksi pada faal tubuh dan menyebabkan terjadinya penyakit yang kronis.
- Pencemaran tingkat keempat; yaitu pencemaran yang telah menimbulkan sakit akut dan kematian bagi manusia maupun hewan dan tumbuh-tumbuhan.
Gas-gas
CO, SO2, H2S, partikulat padat
dan partikulat cair yang dapat mencemari udara secara alami ini disebut bahan
pencemar udara alami, sedangkan yang dihasilkan karena kegiatan
manusia disebut bahan pencemar
buatan.
Sumber bahan pencemar udara ada lima macam yang merupakan
penyebab utama (sekitar 90%) terjadinya pencemaran udara global di seluruh
dunia yaitu:
- Gas karbon monoksida, CO
- Gas-gas nitrogen oksida, NOx
- Gas hidrokarbon, CH
- Gas belerang oksida, SOx
- Partikulat-partikulat (padat dan cair)
Gas karbon monoksida merupakan
bahan pencemar yang paling banyak terdapat di udara, sedangkan bahan pencemar
berupa partikulat (padat maupun cair) merupakan bahan pencemar yang sangat
berbahaya (sifat racunnya sekitar 107 kali dari sifat racunnya gas karbon
monoksida).
a. Gas karbon monoksida, CO
Karbon monoksida adalah gas
yang tidak berwarna, tidak berbau, tidak mempunyai rasa, titik didih -192º C,
tidak larut dalam air dan beratnya 96,5% dari berat udara. Reaksi-reaksi yang
menghasilkan gas karbon monoksida antara lain:
- Pembakaran tidak sempurna dari bahan bakar atau senyawa senyawa karbon lainnya:
2 C + O 2 ? 2 CO
- Reaksi antara gas karbon dioksida dengan karbon dalam proses industri yang terjadi dalam tanur:
CO2 + C ? 2 CO
- Penguraian gas karbon dioksida pada suhu tinggi:
2 CO2 ? 2 CO + O 2
- Gas karbon monoksida yang dihasilkan secara alami yang masuk ke atmosfer lebih sedikit bila dibandingkan dengan yang dihasilkan dari kegiatan manusia.
b. Gas-gas Nitrogen oksida, NOx
Gas-gas Nitrogen oksida yang
ada di udara adalah Nitrogen monoksida NO, dan Nitrogen dioksida NO2 termasuk
bahan pencemar udara. Gas Nitrogen monoksida tidak berwarna, tidak berbau,
tetapi gas nitrogen dioksida berwarna coklat kemerahan dan berbau tajam dan
menyebabkan orang menjadi lemas. Reaksi-reaksi yang menghasilkan gas NO dan NO2
antara lain:
(1210 – 1765)ºC
2 N + O2 ? 2 NO
2 NO + O2 ? 2 NO
c. Hidrokarbon CH
Sumber terbesar senyawa
hidrokarbon adalah tumbuhtumbuhan. Gas metana CH4 adalah senyawa hidrokarbon
yang banyak dihasilkan dari penguraian senyawa organik oleh bakteri anaerob
yang terjadi dalam air, dalam tanah dan dalam sedimen yang masuk ke dalam
lapisan atmosfer:
2 (CH2O)n ? CO2 + CH4
d. Gas-gas belerang oksida SOx
Gas belerang dioksida SO2
tidak berwarna, dan berbau sangat tajam. Gas belerang dioksida dihasilkan dari
pembakaran senyawasenyawa yang mengandung unsur belerang. Gas belerang
dioksida SO2 terdapat di udara biasanya bercampur dengan gas belerang trioksida
SO3 dan campuran ini diberi simbol sebagai SOx.
S + O2 ? SO2
2 SO2 + O 2 ? 2 SO3
e. Partikulat
Yang dimaksud dengan
partikulat adalah berupa butiran-butiran kecil zat padat dan tetes-tetes air.
Partikulat-partikulat ini banyak terdapat dalam lapisan atmosfer dan merupakan
bahan pencemar udara yang sangat berbahaya.
Di atas telah Anda pelajari
bahwa pencemaran udara dapat memberikan dampak negatif bagi makhluk hidup,
manusia, hewan dan tumbuh-tumbuhan. Kebakaran hutan dan gunung api yang meletus
menyebabkan banyak hewan yang kehilangan tempat berlindung, banyak hewan dan
tumbuhan mati bahkan punah. Gas-gas oksida belerang (SO2 dan SO3) bereaksi dengan uap
air, dan air hujan dapat menyebabkan terjadinya hujan asam yang dapat merusak
gedung-gedung, jembatan, patung-patung sehingga mengakibatkan tumbuhan mati atau
tidak bisa tumbuh. Gas karbon monoksida bila terhisap masuk ke dalam paru-paru
bereaksi dengan haemoglobin menyebabkan terjadinya keracunan darah dan masih
banyak lagi dampak negatif yang disebabkan oleh pencemaran udara.
a.Satuan-satuan
pengukuran pencemaran
Kuantitas pencemaran dapat
dinyatakan atasa dasar volume atau dasar massa. Untuk yang berdasarkan massa,
satuan yang tepatialah gram/cm3 atau pon massa ft3. Satuan volumetric biasa
digunakan sebagai bagian per sejuta(part per million,atau ppm) yang
didefinisikan sebagai :
1 ppm = 1 volume gas pencemar
Atau 0,0001 persen volume = 1ppm
Untuk mengubah satuan volumetric
menjadfi satuan berdasarkan massa,kita tentu harus mengetahui bobot molekul bahan
pencemar itu agar dapat menghitung volumenya pada suhu dan tekanan
tertentu.Andaikan perangai gas ideal,konversi itu dilakukan dengan

Dimana :
mp/v = konsentarasi masa pencemar(kg/m3)
Mp = bobot molekul pencemar (gr/mol)
P = tekanan total campuran udara dan zat
pencemar(atm)
R = konstanta gas universal
T =
suhu absolute campuran(K)
Satuan yang lebih umum adalah
microgram per meter kubik.
1kg/m3 = 109g/m3
Konsentrasi-konsentrasi
volumetric dan massa yang setara untuk beberapa zat pencemar biasa dib erikan
table 7-1
Tabel 7-1 konsentrasi massa 1ppm zat pencemar biasa pada 1 atm
Zat Pencemar
|
Konsentrasi massa
(g/m3)
|
|
0o
|
25o
|
|
Karbon monoksida(CO)
|
1250
|
1145
|
Nitrogen oksida(NO)
|
-
|
1230
|
Nitrogen dioksida(NO2)
|
-
|
1880
|
Ozon(03)
|
2141
|
1962
|
PAN[CH3(CO)O2NO2]
|
5398
|
4945
|
Sulfur dioksida(SO2)
|
2860
|
2620
|
b.Rentet Umum Pengambilan Contoh Udara
Pada gambar
7-1 diperlihatakan rentet umum
pengambilan contoh udara.Tidak semua penerapan harus
Menggunakan keseluruhan unsure
perangkat itu.Perangkap pengambilan contoh terdiri dari 4 bagian dasar :
1.Peranti –peranti persiapan
Contoh
2.Peralatan pengambilan contoh
3.Peranti ukur
4.Sumber vakum
Peranti-peranti
persiapan contoh mengubah contoh masuk sehingga komponen gas atau partikel yang
dikehendaki dapat dikumpulkan dengan mudah .Persiapan itu terdiri dari :
1.Penyaringan
2.Pengeringan untuk mengeluarkan kelembaban
3.Penjenuhan dengan uap air
4.Berbagai reaksi untuk
mengeluarkan bahan pencemar yang tidak dikehendaki yang dapat mengganggu
pengukuran nanti.
Dalam
berbagai pengumpulan contoh,pencemaran berbentuk gas atau butifran dikeluarkan
dari udara dengan salah satu metode
dibawah ini :
Pengumpulan gas:
>Adsorpsi pada permukaan zat
padat
>Absorpsi dengan reaksi kimia
ke dalam zat cair
>kondensdasi kedalam perangkap
beku pisah
Pengumpulan butiran:
>penyaringan
>pemisahan dengan
sedimentasi(pengendapan)
Jika
sudah terkumpul,contoh diukur secara kuantitatif,sesudah pengumpulan
contoh,laju aliran,suhu dan tekanan
diukur dengan metode-metode yang telah diuraikan pada bahaasan pokok
terdahulu.Udara ditarik dengan bantuan
sumber penghampa(vakum).Untuk melindungi sumber vakum itu,pada pengukuran
dipasang penyaringan atau pemisah.Sebagai catatan bahwa semua penghubung harus
bersifat nonreaktif terhadap zat pencemar yang akan diukur.
c.Teknik Pengambilan Contoh
Ada beberapa metode untuk menumpulkan
contoh-contoh berwujud gas dari contoh udara:
1.Teknik Absorbsi
Dalam teknik absorpsi ini contoh udara
dibuat menggelembung –gelembung melalui zat cair tertentu sehingga zat pencemar
yang dikandungnya diserap dengan reaksi kimia. Proses absorbsi terjadi didalam
kolom absorbsi yang berbentuk silinder. Laju absorbsi dipengaruhi oleh laju
aliran gas melalui absorber, konsentrasi larutan penyerap dan waktu kontak
menyeluruh. Setelah diserap zat cair pereaksi itu dianalisis untuk menentukan
konsentrasi komponen yang sebanding dengan gas pencemarsemula.
2.Teknik Adsorbsi
Dalam proses adsorbsi molekul gas yang
akan dianalisis ditempatkan dalam keadaan kontak dengan permukaan zat padat,
dimana molekul gas itu melekat. Contoh zat padat yang biasa digunakan dalam
proses ini adalah karbon aktif, alumina(AlO2) aktif, dan gel silika
(SiO2). Zat padat itu dapat dicuci dengan zat pereaksi yang lalu
menyerap (adsorbsi) pencemar yang kemudian dianalisis.
3.Teknik Kondensasi dan Teknik Beku Pisah
Jika contoh udara itu dilewatkan melalui
kamar-kamar pendingin yang dijaga pada suhu sangat. Hal ini dapat menyebabkan
berbagai komponen gas itu mengkondensasi atau membeku dan terpisah.
d. Teknik pengambilan contoh butiran
Ukuran bahan-bahan butiran yang ditemukan
dalam pencemaran udara sangat bervariasi berkisar 0,001 sampai 500 µm, dimana
kebanyakan partikel atmosfer jauth diantara 0,1 dan 10 µm.untuk partikel yang
sangat kecil yaitu dibawah 0,1 µm, gerakkan dan perpindahan sangat ditentukan
oleh tumbukan molekul, sedang yang lebih besar dari 20 µm cenderung untuk
mengendap keluar dari atmosfer dan mengumpul lingkungan lokalnya.
1. Pengendapan dan sedimentasi
Salah satu mekanisme pengumpulan contoh
lain ialah berupa bejana sederhana yang diletakkan di tempat yang tepat dan
mengamatinya setelah beberapa waktu.jadi pencemaran butiran dari pabrik
pengecoran besi diukur dengan menempatkan sebuah bejana disekitar pabrik itu
dan mengukur akumulasi butiran setelah beberapa hari.
2.Pengumpulan dengan cara mekanik
Contoh gas dikumpulkan dalam bejana yang
terlebih dahulu divakumkan dan ditutup. Setelah terkumpul, contoh itu lalu
sianalisis si laboratorium.
3.Teknik filtrasi
Dengan menggunakan sumber vakumperangkat
pengambilan contoh, Kita dapat melewatkan suatu volume tertentuudara melintasi
penyaring(filter) yang tepat untuk mengumpulkan benda-benda butiran.setelah
beberapa waktu, dikeluarkan dan dibawa ke laboratorium untuk diperiksa.
Salah satu teknik pengumpulan dengan
filtrasi menggunakan pengambil contoh volume besar yang dilengkapi dengan motor
sapu penyedot debu untuk menarik contoh itu melintas filter besar yang terbuat
dari kertas serat.
4.Kolektor tubruk dan presipitator
Dalam piranti pengumpulan contoh yang bekerja
atas dasar tubrukan, contoh udara mula-mula dipercepat hingga kecepatan tinggi
lalu dipaksa mengalami perubahan arah dengan cepat.dalam beberapa piranti
tertentu permukaan itu dibuat basah dan butiran-butiran yang terkumpul dibuat
dihanyutkan dengan zat cair itu. Pada piranti yang kering, biasanya digunakan
susunan kaskade, dimana arus itu mendapat kecepatan yang makin lama makin
tinggi, dan dengan demikian memisahkan butiran-butiran yang makin kecil pula.
Presipitator elektrostatik merupakan alat
yang paling efisien untuk mengumpulkan partikel. Contoh udara dihisap melalui
kisi kawat yang bermuatan 12 sampai 30 kV. Partikel-partikel itu menjadi
bermuatan pula, dan selanjutnya dikumpulkan pada plat pengumpul yang mempunyai
muatan berlawanan. Bila piranti itu dimatikan, partikel-partikel itu dapat
dikeluarkan dari plat dan dianalisa di laboratorium.
e.Pengukuran Sulfur Dioksida
Ada beberapa teknik yang digunakan untuk
pengukuran SO2 sulfur dioksida tinul sebagai akibat pembakaran bahan
hidrokarbon yang mengandung banyak belerang dan merupakan suatu sumber utama
pencemaran udara. Oleh karena itu banyaknya industri yang membakar batu bara
atau minyak baker yang mengandung kadar belerang tinggi, teknik-teknik
pengukuran ini luas juga penerapannya.
1.Analisa SO2 Dengan Cara Kolorimetri
Dalam gambar 7-2 digambarkan apparatus
dasar untuk penentuan SO2 dengan kolorimetri. Contoh udara ditarik dengan pompa
vakum melalui piranti pengukuran aliran
masuk dan kemudian masuk ke pembasuh piring berputar. Permukaan piring-piring
itu dibasahi dengan penyerap sehingga terdapat permukaan yang luas untuk
bersinggungan dengan gas. Hal ini menyebabkan kecepatan dan tanggapan absorbsi
menjadi tinggi pula. Larutan sekarang yang mengandung pencemar lalu dicampur
dengan pereaksi pararosalina putih dan dibiarkan mengalir melalui lilitan untuk
memberi waktu bagi berkembangnya rekasi pembentukan warna.
Sumber cahaya disaring dan dilewatkan
melalui pemenggal yang dijalankan dengan motor untuk mendapatkan sumber
bolak-balik yang dapat diamplikasikan secara elektronik. Dua fotosel
cadmium-sulfida yang sepasang digunakan untuk mengindera transmisi cahaya dari
sel pengindera yang berisi contoh itu, yang telah mengalami reaksi kolorimetri
dan juga dari sel rujukan yang berisi zat pereaksi (reagent). Keluaran kedua
sel itu dibandingkan dengan rangkaian deteksi elektronik yang mengirimkan pula
tegangan keluaran ke suatu perekam.
Skema
Penentuan SO2 secara Kolorimetri
2.Analisa SO2 Cara Elektrokonduktivitas
Pengukuran elektrokonduktivitas
menghasilkan ion sulfat yang mengubah
konduktivitas
larutan, sebanding dengan SO2 yang ada. Dengan menggunakan air
sebagai
pereaksi kita dapatkan reaksi:
H2O +SO2 ──►H2SO3
H2SO3 +1/2 O2
──►H2SO4
sebagai
alternatif kita dapat memakai H2O2 dalam hal ini, kita tidak akan mengalami
banyak gangguan dari gas-gas seperti CO2
H2O2+SO2──► H2SO4
Prinsip kerjanya ialah zat
pereaksi dilewattkan terlebih dahulu melalui sel rujukan, kemudian melalui
kolom absorbsi dimana contoh udara itu bercampur di dalam proses aliran arus
berlawanan. SO2 diserap di dalam pereaksi, dan larutan baru yang terjadi
dilewatkan melalui sel pengukur konduktivitas. Pada sel konduktivitas itu
diberikan tegangan arus bolak-balik dan arusnya diukur untuk menghitung tahanannnya.
kalibrasi tingkat nol dilakukan dengan mengalirkan udara tersebut melalui kapur soda untuk
memisahkan semua SO2 untuk kondisi ini. Konduktivitas sel rujukan
dan sel pengukur harus sama dan karena itu dapat dipakai untuk menetapkan
tingkat keluaran.
3.Analisa SO2 Cara Coulometri
Untuk melakukan anlisi dengan
coulometri, sel detector dibuat seperti pada gambar. sel tersebut mengandung
larutan dapar KI yang membangkitkan I2 pada anoda menurut persamaan reaksi:
2I- ──►I2 +2e
Bila contoh udara yang mengandung
SO2 ditarik ke dalam sel itu, maka ia bereaksi dengan I2
sehungga dipisahkan dari sel. I2 yang tidak bereaksi kemudian
direduksi menjadi I- pada katoda. Sebagai akibat reaksi itu, elektroda rujukan
akan dapat mendeteksi perbedaan antara arus anoda dan katoda sebagai berikut:
Ir = Ia –
Ic
Arus ini kemudian diperkuat untuk
mendapatkan keluaran yang sebanding dengan konsentrasi SO2.
f.Pengukuran Hasil Pembakaran
Analisa hasil pembakaran tidak
saja penting untuk pengendalaian pencemaran udara, tetapi juga untuk menjaga
agar laju pembakaran dan penggunaan energi berlangsung efisien.
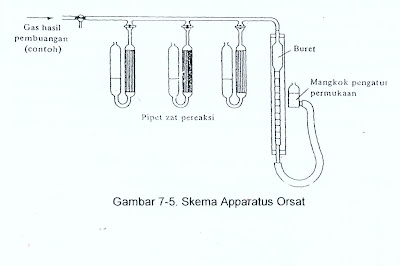
Pada gambar 7-5 terlihat
apparatus sederhana yang digunakan untuk menganalisis hasil pembakaran. Alat
itu terdiri dari sebuah buret ukur dan tiga buah pipet pereaksi yang digunakan
berturut-turut untuk menyerap karbon dioksida, oksigen, dan karbon
monoksidadari campuran itu. Mula-mula hasil pembakaran ditarik kedalam buret
ukur. Kemudian manifold pengambilan contoh ditutup dan contoh itu didorong masuk
ke pipet pereaksi pertama, dimana karbo dioksida diserap. Contoh itu
dikembalikan ke buret ukur dan penurunan volume dicatat. Prosedur ini diulangi
lagi dengan kedua pipet berikutnya. Yang masing-masiing secara berturut-turut
menyerap O2 dan CO. dalam proses pengukuran
volumetric zat-zat tersebut didapatkan atas dasar kering artinya tanpa
memperhitungkan uap air yang ada.
Sebagai pereaksi biasanya
digunakan kalium hoidroksida untuk menyerap karbon dioksida. Untuk menyerap
oksigen digunakan campuran asam pirogalat dan larutan kalium hidroksida, sedang
kupro klorida digunakan untuk menyerap karbon monoksida.
g. Pengukuran keburaman
Keburaman
arus gas yang keluar dari cerobong asap memang merupakan ukuran
konsentrasi zat butiran didalam gas itu.Namun
warna gas buangan bergantung pada bahan butirana apa yang terdapat dalam proses
itu.
Ungtuk
membantu penmbakuan pengamatan visual telah dikembangkan system peta asap
ringleman.lima buah cart disusun denagn peningkatan kehitaman yang teratur
seperti terlihat pada table 7-2./Pengamatan lalu dilatih untuk membandingkan
pengamatannya dengan cart tersebut.Daalam proses latihan,cart tersebut
ditempatkan pada jarak 50ft dari pengamatan,pada garis pandang yang sama denagn
asap itu.pada jarak itu,cart-cart terssebut akan tampak seperti beberapa tingkat keabu-abuan.dalam pengamatan
itu,pengamat harus berdiri membelakangi matahari.Untuk latihan,pengukuran
trabsmisi optic dapat pula dilaakukan pada asap untuk dikolerasikan.
Tabel 7-2 garis pisah untuk pembuatan cart
Cart Ringleman
|
Tebal garis hitam,mm
|
Tebal bidang putih,mm
|
% hitam
|
0
|
Putih semua
|
0
|
|
1
|
1
|
9
|
20
|
2
|
2,3
|
7,7
|
40
|
3
|
3,7
|
6,3
|
60
|
4
|
5,5
|
4,5
|
80
|
5
|
Hitam semua
|
100
|
Keburaman
buangan cerobong dapat dengan mudah diubah tanpa mengubah emisi total
pencemar.Oleh karena keburaman merupakan fungsi
dari panjang lintas optic,salah satu cara untuk mengubah keburaman ialah
memperkecil diameter cerobong dan meningkatkan kecepatan aliran.cara lain ialah menambah jumlah cerobong yang
digunakan.peraturan-peraturan pengenddalian
pencemaran udara sering tidak memungkinkan penggunaan teknik-teknik tersebut
bila pabrik itu sudah dituduh mempunyai keburaman buangan terlalu tinggi.
h. Pengukuran Bau
Setiap
orang akan berbeda reaksinya mengenai bau tertentu.Secara ideal,kita tentu
ingin menyatakan tingkat abau dengan konsentrasi zat bau dalam bagian persejuta(ppm) atau microgram permeter
kubik.Teknik yang biasa digunakan ialah memberikan berbagai konsentrasi zat bau kepada sekelompok orang dan meminta
setiap anggota kelompom itu memberikan penilaian denagn skala :
5
Bau tak tertahankan
4
Sangat berbau
3
Bau mudah tercium
2
Agak berbau
1
Hampir tidak berbau
0
tidak berbau
Skala
ini dapat diterapkan terhadap intensitas bau,mudahnya bau itu menjalar dan
tingkat bau itu disukai atau tidak disukai.
P=K log S
Bila data telah
terkumpul,memenuhi hubungan,dimana P adalah respon indra manusia,atau
intensitas(dari 0 sampai 5),dan S adalah rasio konsentrasi dalam bagian
persejuta terhadap respon 0.K ialah konstanta yang besarnya antara 0,3 dan
0,6,bergantung pada jenis zat bau.Dengan menggunakan teknik-teknik seperti
itu,kita dapat menentukan ambang bau berbagai zat,seperti pada table 7-3.
1 satuan bau=kunatitas zat bau
yang mencemarkan 1 ft3 udara bersih untuk mencapai nilai ambang.
Dari
table 7-3 bisa diliihat bahwa 1 satuan bau aseton ialah kuantitas yang
diperlukan untuk menghasilkkan konsentrasi
100 ppm,sedang satu satuan bau formaldehidaiaalah kuantitas yang
diperlukan untuk menghasilkan konsentrasi 1,0 ppm.
Tabel 7-3.Ambang bau di udara
Zat bau
|
Ambang bau,ppm
|
Asam asetat
|
1,0
|
Aseton
|
100
|
Amina trimetril
|
0,0021
|
Amonia
|
46,8
|
Anilina
|
1,0
|
Karbon disulfide
|
0,21
|
Klor
|
0,31
|
Dietil formanida
|
100
|
Difenil sulfida
|
0,21
|
Formaldehida
|
1,0
|
Hydrogen sulfide
|
0,00047
|
Methanol
|
100
|
Metilena klorida
|
214
|
Nitrobenzene
|
0,00047
|
Fenol
|
0,047
|
Trimetil amina
|
0,00021
|
III.Penutup
a.Kesimpulan
Dalam makalah ini dapat
disimpulkan betapa pentingnya pengukuran pencemaran udara sebab dengan
melakukan pengukuran kita dapat menetapkan tingkat pencemaran udara di suatu
tempat dengan memperhatikan data biologi yang menerima dampak pencemaran udara
secara langsung seperti manusia dan hewan. Selain itu kita juga dapat
menentukan sumber-sumber penyebab pencemaran udara sehingga kita dapat
menentukan derajat pengendalian yang diperlukan.
Dalam melakukan pengukuran
kita harus mengambil contoh udara yang akan diteliti sehingga kita dapat
mengetahui apakah di daerah tersebut telah terjadi pencemaran udara atau tidak.
Pengambilan contoh dilakukan oleh perangkat pengambilan contoh yang terdiri
dari 4 bagian yaitu piranti persiapan contoh, peralatan pengumpulan contoh,
peranti ukur dan sumber vakum.
Untuk melakukan pengambilan
contoh udara diperlukan suatu teknik yang tepat agar kiata dapat menegtahui
bahan pencemar apa saja yang terdapat diudara. Berdasrkan bentuknya teknik
pengambilan contoh dibagi menjadi 2 yaitu teknik pengambialn contoh udara
yang berbentuk gas dan yang berbentuk
butiran. Pada teknik pengambilan contoh udara berbentuk gas dibagi menjadi 3
yaitu teknik absorbsi, teknik adsorbsi, dan teknik perangkap beku pisah
sedangkan pada megambilan contoh udara yang berbentuk butiran dibagi menjadi 4
yaitu pengendapan dan sedimentasi, pengumpilan dengan cara mekanik, reknik sedimentasi
dan teknik kolektor tubruk dan presipitator.
Dalam pencemaran udara banyak
sekali zat yang menyebabkan udara tercemar dan salah satu yang berbahaya adalah
sulfur dioksida yang dapat menyebabkan hujan asam selain itu zat ini merupakan zat pencemar yang paling banyak
dihasilkan oleh banyak industri selain gas CO dan CO2 oleh karena itu
diperlukan teknik khusus untuk pengukur tingkat pencemaran yang disebabkan loeh
gas sulfur dioksida. Dalam pengukuran sulfur dioksida dikenal 3 metode umum
yaitu analisa dengan cara kolorimetri, dengan cara elektrokondutivitas dan
terakhir dengan cara coulometri.
Selain bahan pencemar
indicator lain yang perlu diukur dalam pengukuran pencemaran udara yaitu
pembakaran, keburaman, dan bau. Pembakaran dan keburaman perlu diukur untuk
mengetahui seberapa sempurna pembakaran itu apabila pembakaran itu tidak
sempurna maka akan banyak sekali zat pencemar yang terdapat didalamnya yang
menyebabkan hasil pembakaran berwarna hitam pekat atau buram.




ijin menyimak
ReplyDeletemonggo mas...
Deletereferensinya dari mana mas ?
ReplyDelete